El Boceprevir es un inhibidor de la proteasa NS3 del VHC, que ha sido desarrollado por Schering-Plough, compañía que recientemente se ha integrado en la farmacéutica Merck. Se administra por via oral.La dosis de boceprevir fue de 800mg tres veces al dia.
Los objetivos del estudio fueron comparar la eficacia y seguridad de dos estrategias terapéuticas con boceprevir + (interferon pegilado) INF+ ribavirina (RBV) frente a un tratamiento estándar con INF+RBV en paceintes infectados por el VHC genotipo 1.
Se evaluaron estás estrategias en dos cohortes determinadas ( personas de raza negra y raza blanca).
Por último se exploraron dos estrategias: en una se utilizó boceprevir durante 24 semanas, y según la respuesta ampliar a 44 semanas de tratamiento y en la otra se utilizó tratamiento durante 44 semanas con boceprevir.
- El objetivo primario fue la RVS a la semana 24 en un análisis por intención de tratar.
- El objetivo secundario fue la RVS a la semana 24 en un análisis por intención de tratar modificado: incluía únicamente aquellos pacientes que recibieron mas de una dosis de boceprevir.
En las tres ramas del estudio (360 pacientes/rama) se administró tratamiento con INF y RBV durante el primer mes, y a partir de entonces según la rama:
- Se continuó con el mismo tratamiento hasta la semana 48.
- Se añadió al tratamiento estándar Boceprevir hasta la semana 28 (en esta rama, los pacientes que entre la semana 8 y 24 estuvieron detectables se les añadió de nuevo tratamiento con INF+RBV hasta la semana 48)
- Se añadió al tratamiento estándar Boceprevir hasta la semana 48
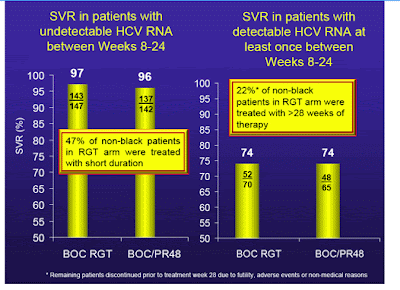
A continuación se muestran los resultados del estudio: La utilización de boceprevir durante 24 semanas es igual de eficaz que la utilización boceprevir durante 44 semanas
Por último se exploraron dos estrategias: en una se utilizó boceprevir durante 24 semanas, y según la respuesta ampliar a 44 semanas de tratamiento y en la otra se utilizó tratamiento durante 44 semanas con boceprevir.
La utilización de boceprevir durante 24 semanas es igual de eficaz que la utilización boceprevir durante 44 semanas.
La respuesta de INF+RBV durante el primer mes de tratamiento, permite predecir la RVS (basado en el grado de respuesta temprana) y permite determinar la probabilidad de desarrollar resistencias al boceprevir.
Los abandonos por efectos adversos relacionados con la anemia no fueron frecuentes (<2%).











No hay comentarios:
Publicar un comentario